王哲医生的科普号
- 精选 前列腺癌的骨转移4(检查)
单光子发射X射线计算机断层成像(single photon emission computed tomography,SPECT):锝-99亚甲基二磷酸盐(99mTc-MDP)SPECT全身骨显像是前列腺癌骨转移首选的筛查方法,可早期发现骨转移灶。
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科1089人已读 - 精选 前列腺癌的骨转移3(症状)
早期前列腺癌通常没有症状,部分晚期患者因骨痛而就诊。超过3/4的前列腺癌患者会出现骨转移,大约50%的患者初诊时即有骨转移的发生。前列腺骨转移好发于骨盆,其次为脊柱,颅骨转移者少见,在外周骨中最易转移至四肢骨,其中以股骨最为多见。骨转移灶会引起病理性骨折及脊髓压迫等症状。广泛骨转移患者容易出现疲劳、消瘦、贫血等症状,严重者可能出现全身器官功能衰竭。
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科2061人已读 - 医学科普 前列腺肉瘤病理特点
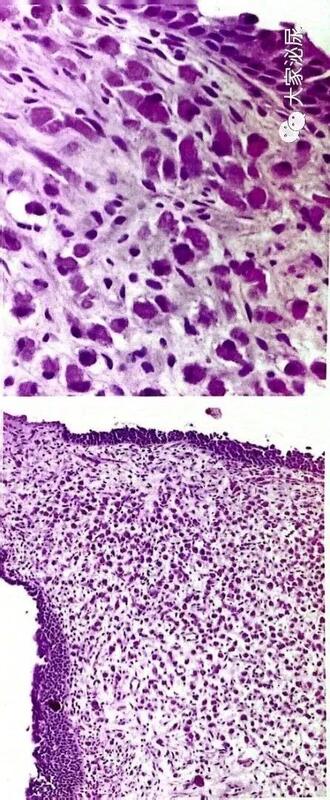
1.前列腺横纹肌肉瘤前列腺横纹肌肉瘤:是一类具有横纹肌分化、原发于前列腺组织的肌源性肉瘤。前列腺横纹肌肉瘤是儿童时期最常见的前列腺恶性肿瘤,发生于幼儿期至成年早期,平均诊断年龄为5岁,而在成人中,患者的诊断年龄从17岁到68岁不等,该肿瘤通常体积较大,表现为向前列腺周围扩张生长。横纹肌肉瘤(图1)由原始的未分化的圆形-梭形细胞组成,无明显或仅有局灶性横纹肌肉瘤细胞分化,在组织学上可表现为胚胎性横纹肌肉瘤、梭形细胞或多形性横纹肌肉瘤,少数为腺泡状横纹肌肉瘤。胚胎横纹肌肉瘤主要由幼稚分化的小圆细胞及胞质较小的短小梭形细胞组成,部分胞质较红染,其中可见横纹肌母细胞;多形性横纹肌肉瘤细胞多型性明显,主要为大梭形细胞及带状细胞;腺泡状横纹肌肉瘤通过FISH试验可检测到特异性的染色体异位t(2;13)(q35;q14),t(1;13)(p36;q14),存在PAX3/7-FOXO1基因融合。图1:前列腺横纹肌肉瘤(HE染色)前列腺横纹肌肉瘤免疫组织化学染色包括Vimentin、Myoglobin、Desmin、Muscle、Actin、MYF-4表达阳性,CK、CD34表达阴性,Ki-67指数>90%,有报道表明Myod1和Myogenin是敏感性和特异性最高的标志物。2.前列腺平滑肌肉瘤前列腺平滑肌肉瘤:是一类罕见的恶性平滑肌肿瘤,表现为平滑肌分化。前列腺平滑肌肉瘤为成人前列腺最常见的肉瘤类型,患者大多分布于40-70岁,肿瘤大小在3~20cm,常取代整个前列腺并侵犯到前列腺外。前列腺平滑肌肉瘤(图2)同其他部位的平滑肌肉瘤相似,从表现为中度异型性的平滑肌肿瘤到多形性肉瘤不等,且可能存在广泛的肿瘤组织坏死,其镜下细胞多呈梭形,分化较好的肿瘤细胞以长梭形为主,胞质丰富且嗜酸性红染,部分细胞可见有丝分裂,而分化差的细胞表现为多型性,核分裂象多,中到重度的核异型性,偶可见瘤巨细胞核,部分标本可见明显的平滑肌分化特征。前列腺平滑肌肉瘤与非典型平滑肌瘤的鉴别标准与其他器官相似,包括异型性、细胞结构、坏死情况和有丝分裂活动。前列腺平滑肌肉瘤对平滑肌特异性肌动蛋白和波形蛋白有免疫反应,在一些患者中还存在有结蛋白、细胞角蛋白和S100的局部表达。免疫组化表现为Vimentin、Desmin、Muscle、Actin阳性,Myoglobin、CK、CD34、PSA表达阴性。图2:前列腺平滑肌肉瘤(HE染色)3.前列腺间质肉瘤前列腺间质肉瘤:是来源于前列腺特异性间质的肉瘤,患者发病年龄轻,半数以上的间质肉瘤患者发病于50岁之前。间质肉瘤表现为实性或部分囊性的界限欠清的前列腺实质性肿块,囊性变对应于相应的叶状型组织学构型,肿瘤直径2~18cm,切面灰白,灰黄,其中出血、坏死较常见。在组织学上,间质肉瘤表现为间质过度增生伴或不伴有内陷的良性腺体,细胞密度增加,瘤细胞具有明显的多形性和活跃的核分裂活性。组织构型上,双向型叶状肿瘤最为常见,表现为肉瘤样的间质伴有内陷的良性前列腺腺体形成类似于乳腺叶状肿瘤的分叶状结构,其他组织学构型包括席纹状、纤维肉瘤样及无结构的排列方式,偶尔肿瘤细胞可表现为上皮样或横纹肌样细胞表型。在实际诊断过程中,依据肿瘤细胞的异型性程度,核分裂象的多少及有无肿瘤性坏死,间质肉瘤通常分为高级别和低级别间质肉瘤,但是目前还没有严格界定低级别和高级别间质肉瘤的具体量化标准,一般来说高级别肉瘤具有中-重度的细胞异型性,明显升高的核分裂象和存在肿瘤性坏死。前列腺间质肉瘤表达Vimentin、CD34及PR,不同程度表达SMA、Desmin及MSA,一般不表达ER、S100、c-kit。叶状型肿瘤中的上皮成分表达PSA。4.前列腺纤维肉瘤前列腺纤维肉瘤:其细胞呈束状排列,部分区域可见席纹样结构,细胞核深色,核分裂象较多,偶可见泡沫样细胞。免疫组化常表现为Vimentin、Desmin、αl-AT、αl-ACT和Lysozyme表达阳性。5.前列腺滑膜肉瘤前列腺滑膜肉瘤:其表现为梭形细胞和卵圆细胞交织成束形成的类似纤维肉瘤,Vimentin表达阳性,Desmin及S100表达阴性。与其他部位的软组织滑膜肉瘤相同,通过FISH试验也发现染色体异位t(x;18)(p11.2;q11.2)。6.前列腺骨源性肉瘤前列腺骨源性肉瘤:其常表现为除梭形细胞和多型性细胞外,肿瘤还可见钙化的类骨质,上皮抗原、细胞角蛋白、Vimentin表表达阳性。7.前列腺梭形细胞肉瘤前列腺梭形细胞肉瘤:其组织中可包含有高级别上皮癌成分,Vimentin、Desmin、Muscle、Actin表达均为阴性,Ki-67指数2%。
 王哲 副主任医师 河北北方学院附属第一医院 泌尿外科148人已读
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科148人已读 - 医学科普 转移性前列腺癌中发生前列腺导管内癌的危险因素
前列腺导管内癌(intraductalcarcinomaoftheprostate,IDC-P)是一种独特的组织病理学类型,主要由膨胀性增殖的前列腺导管内恶性上皮细胞构成,但其又与正常导管小叶结构类似,并未破坏周围的基底细胞层。IDC-P常与浸润性前列腺腺泡腺癌并存,有学者认为这种现象是高级别腺泡腺癌浸润导管所致。但与之相悖的是少数IDC-P不伴有浸润性前列腺腺泡腺癌,被称为孤立性IDC-P,其在前列腺癌中的检出率为0.06%~0.26%[1-2]。IDC-P与不良预后密切相关,研究结果显示IDC-P具有侵袭性的分子特征,常与PTEN缺失、BRCA2突变和基因组不稳定性相关[3-5]。研究结果显示,IDC-P与肿瘤体积大、Gleason评分高、神经脉管浸润、前列腺包膜和精囊腺侵犯相关,且与生化复发和疾病无进展生存期呈明显负相关[6-7]。此外,IDC-P是预测放疗后早期(<36个月)生化复发的独立指标,进展至去势抵抗性前列腺癌的时间显著缩短[8]。因此,在前列腺穿刺活检病理标本中准确识别和报告IDC-P至关重要。由于对IDC-P认识不足,我国实际临床工作中IDC-P的病理报告率仅为6%[9],远低于文献报道的穿刺标本中13.7%的阳性率[10],提示可能存在漏诊情况。
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科163人已读 - 学术前沿 mCRPC的序贯治疗,2023ASCO-GU观点
mCRPC患者治疗方式的序贯及组合—ASCOGU2023最新观点转移性去势抵抗性前列腺癌(mCRPC)是前列腺癌的终末阶段。尽管如此,mCRPC阶段的治疗手段仍十分丰富,包括:新型内分泌治疗(阿比特龙、恩扎卢胺),紫杉烷类化疗(多西他赛、卡巴他赛),靶向治疗(PARPi,AKTinhibitor)及核素治疗(镭223、镥177)等。那么,如何序贯或者组合上述治疗才能实现mCRPC患者生存获益的最大化是值得我们思考的问题,尤其是在转移性激素敏感性前列腺癌(mHPSC)的治疗由过去的单纯内分泌治疗(ADT)进入组合治疗模式(ADT+多西他赛或ADT+新型内分泌治疗或三者联合)后。mCRPC阶段治疗手段丰富,如何序贯?如何组合?2023年ASCOGU会议上,来自瑞士的Gillessen教授就当下最前沿的研究总结了mCRPC患者治疗和序贯的模式,值得我们借鉴。根据mHSPC阶段所采纳的治疗方式,我们可以将mCRPC患者分为三大类:01mHSPC阶段接受单纯ADT治疗(单纯ADT或CAB方案)这类mCRPC患者建议行同源重组突变基因(HRR,尤其是BRCA)检测。如果患者不伴有HRR突变,一线可选择新型分泌治疗药物(如恩扎卢胺或阿比特龙)。最新研究显示这一阶段如果患者一线选择阿比特龙联合奥拉帕利或者恩扎卢胺联合他拉唑帕利可能会有更大的潜在获益,我们也会再下一期报道中给大家分享这两个研究(PROpel研究和TALAPRO-2研究)。一线治疗失败后,患者可选择多西他赛化疗或者镭223核素治疗,如病情再进展,三线可序贯镥177核素治疗或卡巴他赛化疗。如果患者伴有HRR突变,一线可选择阿比特龙联合奥拉帕利或者恩扎卢胺联合他拉唑帕利,二线选择多西他赛化疗或镭223核素治疗,三线序贯镥177核素治疗或卡巴他赛化疗
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科100人已读 - 医学科普 前列腺癌的遗传因素
前列腺癌的风险因素在全球,前列腺癌的四个最重要的已知风险因素是年龄、祖先、家族癌症史种系遗传变异。年龄年龄是前列腺癌的重要危险因素。前列腺癌在40岁以下的男性中很少见;此后每十年发病率迅速上升。患前列腺癌的总体终生风险为1/8大约10%的前列腺癌病例在56岁以下的男性中被诊断出来,并且代表早发性前列腺癌。来自监测、流行病学和最终结果(SEER)计划的数据显示,早发性前列腺癌正在增加,有证据表明某些病例可能更具侵略性。祖先与美国其他种族群体(非西班牙裔白人,172.6例/100,000名男性;亚洲或太平洋岛民,99.9例/100,000名男性;美洲印第安人或阿拉斯加原住民,55.0例/100,000名男性;和西班牙裔或拉丁裔,79.8例/100,000名男性)。[85]非西班牙裔黑人个体(3.100/000,1名男性)的前列腺癌死亡率也是美国其他种族群体的两倍多(非西班牙裔白人,37.9/100,000名男性;亚洲或太平洋岛民,17.8/100,000男性;美洲印第安人或阿拉斯加原住民,8.6/100,000男性;和西班牙裔或拉丁裔,21.0/100,000男性)。[15]在全球范围内,前列腺癌的发病率和死亡率也因国家而异。总体来说,东亚地区发病率受人种影像较小。家族癌症史前列腺癌具有高度遗传性;据估计,前列腺癌的遗传风险高达60%。5%至10%的前列腺癌病例被认为主要是由高风险遗传因素或前列腺癌易感基因引起的。家族史是前列腺癌的主要危险因素。患有前列腺癌的兄弟或父亲的家族史会增加患前列腺癌的风险,并且风险与受影响亲属的年龄成反比。也就是说诊断年龄越年轻,亲属受影响几率越大。乳腺癌家族史也与前列腺癌风险增加有关。有乳腺癌家族史的人患前列腺癌的风险总体上高出21%,患致命前列腺癌的风险增加34%。与乳腺癌家族史相关的前列腺癌风险增加的一部分可能是由于DNA损伤修复途径中的致病变异,最常见的是BRCA2。有关详细信息,请参阅 BRCA1和BRCA2 部分。家庭中前列腺癌和乳腺癌之间的关联似乎是双向的。在女性中,前列腺癌家族史同样与乳腺癌风险增加有关。种系遗传变异基因组中有多个种系致病变异和单个核苷酸变异与前列腺癌风险有关。有关这些遗传变异的更多信息,请参阅国家人类基因组研究所GWAS目录,有关前列腺癌基因检测的信息,请参阅遗传性前列腺癌基因检测的临床应用部分。越来越多的数据表明,患有至少一种额外原发性恶性肿瘤的前列腺癌患者不成比例地在已知的癌症易感基因(如BRCA2和MLH1)中携带致病变异。多病例家庭中其他癌症的风险一些报告表明,多例前列腺癌家族的亲属患各种其他癌症的风险增加,但这些关联都没有明确建立。
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科26人已读 - 蛋蛋疼痛?警惕睾丸扭转
近日遇到网上的一位患者咨询:“大夫,我儿子说蛋蛋疼痛,这是咋回事,需不需要去医院看一看?”作为一名靠谱的泌尿男科医生,首先应该想到“蛋蛋疼痛”有睾丸扭转的可能,尤其是青春期的男童。于是我马上回拨电话,经过详细问诊后仍然不能完全排除睾丸扭转可能,于是催促家属去当地医院做了睾丸超声检查。当然,睾丸疼痛还有很多其他原因,比如附睾睾丸炎、睾丸损伤、睾丸附件扭转、精索静脉曲张诱发的睾丸痛,或输尿管结石引起的睾丸牵涉痛等等,但务必要警惕睾丸扭转,延误治疗则可能致睾丸坏死,生育力下降,严重损害男性健康。下面我们将详细介绍睾丸扭转这一泌尿外科急性病症。睾丸扭转的病因及危险因素睾丸扭转即精索发生扭转,是睾丸沿中轴发生顺时针或逆时针旋转后出现睾丸缺血性病变。睾丸扭转可发生在任何年龄,12-18岁男童多见,与青春期精索结构发育不良有关,本病好发于夜间,可能与夜间迷走神经张力增高有关,剧烈活动是睾丸扭转发生诱因。睾丸活动度过大、睾丸引带过长、睾丸引带缺如、睾丸附着过高等都是睾丸扭转发病的结构基础。睾丸扭转的表现男童发生一侧的睾丸疼痛,应想到本病可能,应及时就诊,不能耽误,以免发生睾丸坏死。对于睾丸扭转这一疾患,我们常常强调睾丸缺血急救黄金6小时,即在发生睾丸扭转6小时内睾丸复位,一般预后良好。那么是不是超过6个小时,睾丸就一定会发生缺血坏死呢?答案是否定的。睾丸损害程度与扭转后缺血时间和扭转角度均密切相关,文献报道睾丸扭转时间>6h,扭转>360°,睾丸存活率明显降低;睾丸扭转24h后的挽救成功率低于10%;当扭转角度>360°,时间>24h,睾丸留存的概率几乎为零[1,2]。因此对于睾丸扭转的患者,我们提倡越早发现越好,早期手术保留睾丸功能机会越大。近期,我们又遇到两例首发症状并非阴囊疼痛的睾丸扭转,一例首发症状是下腹疼痛,另一例表现为患侧腹股沟疼痛,后因延误诊治,最终致睾丸坏死行睾丸切除术。Anderson报道,22%睾丸扭转有腹痛症状;王富军报道,12%(8/68)以下腹痛、腹股沟疼痛首发症状;美国54例睾丸扭转引起的医疗纠纷案例,发现约31%的患者首发症状不典型,仅表现为腹痛[3,4]。这都是血淋淋的教训,提醒我们务必要做好细致的查体和鉴别诊断,以免漏诊误诊。睾丸扭转的诊断与鉴别阴囊疼痛就诊者首先要想到睾丸扭转,通过详细检查明确诊断,非阴囊疼痛就诊者也要警惕睾丸扭转的发生,重视睾丸的体格检查,做好睾丸抬举试验,重视阴囊超声睾丸血流变化。突发阴囊疼痛+睾丸肿胀压痛+超声下睾丸血供减少或消失,即可确诊本病,如有怀疑,早期阴囊探查术,对病人的预后获益。对于本病不建议进行阴囊CT或MR检查,不仅诊断意义不大,而且延误挽救睾丸时间。一侧的睾丸扭转,建议选择睾丸复位固定术+对侧睾丸固定术;如睾丸坏死,早期行坏死睾丸切除术,对侧睾丸固定术更是必须,如不然健侧睾丸日后发生再扭转,对男性患者的生育力会是致命性打击。睾丸逆时针扭转360°,>24h睾丸复位后观察15分钟仍无缓解,证实睾丸坏死
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科暂无购买 - 【EAU2021】几种少见类型的肾脏肿瘤|肾癌指南
3.4 其他类型的肾脏肿瘤(Other renal tumours) 其他类型的肾脏肿瘤构成其余的肾皮质肿瘤,包括各种罕见的,散发性的和家族性肿瘤、新近描述的肿瘤、以及一组未分类的肿瘤。这些肿瘤的特点在表3.1进行了总结。下面介绍一些临床相关肿瘤和罕见肿瘤。 3.4.1 肾髓质癌(Renal medullary carcinoma, RMC) 肾髓质癌是一种非常罕见的肿瘤,占比不到所有肾细胞癌的0.5%。肾髓质癌主要在有镰状血红蛋白病(包括镰刀型贫血特质)的年轻人(中位年龄28岁)中被诊断出来。肾髓质癌大多是中央型,边界不清。肾髓质癌是最具侵袭性的肾细胞癌之一。大多数患者(大约67%)会出现转移性病灶。即使是看似局灶性的肾髓质癌也可能在不久之内(通常在几周内)就出现大体转移(macrometastases)。 3.4.1.1治疗 在最近的队列研究中,治疗后的肾髓质癌的中位总生存期(OS)为13个月。由于肾髓质癌具有浸润性并且位于肾髓质中央,所以即使在早期,根治性肾切除术(RN)也比肾部分切除术(PN)效果更好。回顾性研究发现,与单独行全身化疗相比(OS=7个月),局部病灶的肾切除术(OS=16.4个月)的总生存期更长。但应用一线化疗药物后能达到客观缓解(OR)的肾髓质癌患者的生存期更长。存在转移的情况下,远处转移灶切除或肾切除对于肾髓质癌的治疗效果尚不明确。 姑息性放疗也可以用来治疗肾髓质癌。它也许能使靶区的肿瘤消退,但不能阻止放射区外的肿瘤组织进展。单一靶向血管生成的疗法(包括酪氨酸激酶抑制剂(TKI)和mTOR抑制剂)对肾髓质癌疗效不佳。针对肾髓质癌的全身治疗方案是联合应用细胞毒药物,这一方案可在约29%的患者达到完全缓解(CR)或部分缓解(PR)。目前没有前瞻性研究去比较不同化疗方案的疗效,但是大多数已发表的研究纳入了包括铂类,紫杉烷类,吉西他滨和/或蒽环类药物的各种组合用药方案。尽管回顾性研究并未发现MVAC方案(甲氨蝶呤,长春碱,阿霉素和顺铂)对肾髓质癌的疗效优于顺铂,紫杉醇和吉西他滨联合用药,但高剂量的MVAC方案对于肾髓质癌也有一定疗效。目前,一些病例报告宣称单独应用抗PD-1药物(免疫检查点疗法)治疗肾髓质癌已取得一定疗效,但尚无足够的研究来确定肾髓质癌对该疗法的应答率。我们应该尽可能的将肾髓质癌患者纳入探索新疗法的临床试验中,尤其是一线化疗(细胞毒药物)治疗失败的病人。 3.4.2 终末期肾病相关性肿瘤(Carcinoma associated with end-stage renal disease); 获得性囊性疾病相关性肾细胞癌(acquired cystic disease-associated RCC) 终末期肾病(ESRD)的典型特征包括:囊性退行性变(获得性囊性肾病[ACKD])和肾细胞癌发病率更高。在大约4%的终末期肾病患者的自体肾中发现了肾细胞癌。他们患肾细胞癌的终生风险(lifetime risk)至少比普通人群高十倍。与散发性肾细胞癌相比,与ESRD相关的肾细胞癌通常是双侧多发,多见于年轻患者(主要是男性),并且侵袭性较小。目前尚不清楚ESRD相关性肿瘤的相对惰性是由于诊断方式还是特定的ACKD相关的分子途径。尽管ESRD相关性肿瘤的组织病理学类型与散发性肾细胞癌的组织病理学类型相似,但乳头状肾细胞癌亚型在ESRD相关性肿瘤中的发生率相对较高。获得性囊性疾病相关性肾细胞癌(ACD-RCC)是仅在终末期肾脏中出现的特定类型。ACD-RCC临床表现为惰性肿瘤。这可能是由于ESRD患者定期随访导致ACD-RCC在早期被发现。 3.4.3 乳头状腺瘤(Papillary adenoma) 根据WHO 2016分类标准,乳头状腺瘤呈低细胞核恶性程度的乳头状或肾小管结构,直径可达15毫米或更小。 3.4.4 遗传性肾癌(Hereditary kidney tumours) 5%到8%的肾细胞癌是遗传性肾癌;迄今为止,有十种与特定胚系突变、组织病理学和合并症相关的遗传性肾细胞癌综合征。家族史,发病年龄和各种综合征的典型病变通常是诊断遗传性肾细胞癌综合征的线索。遗传性肾细胞癌发病年龄为37岁(中位数);70%的遗传性肾细胞癌发病年龄在所有肾细胞癌发病年龄的最低的十分位区间(46岁)内。在以下疾病中发现遗传性肾脏肿瘤:VHL综合征、遗传性pRCC、Birt-Hogg-Dube综合征、遗传性平滑肌瘤和RCC(HLRCC)、结节性硬化、SDH突变、非息肉病性结直肠癌综合征、甲状旁腺功能亢进-下颌肿瘤综合征、PTEN错构瘤综合征(PHTS),3号染色体易位重构(constitutional chromosome 3 translocations)以及家族性非综合征性ccRCC(familial non-syndromic ccRCC)。由于肾髓质癌与遗传性血红蛋白病相关,因此可以将肾髓质癌也归为遗传性肾癌。 遗传性肾癌综合征患者可能需要反复手术。对于大多数遗传性肾癌患者,建议使用保留肾单位的治疗手段。但因为HLRCC和SDH综合征有侵袭性,所以建议这两种肿瘤一经诊断立即进行手术干预。对于其他遗传性肾癌综合征(例如VHL),推荐观察至肿瘤最大直径达3 cm,以减少外科干预。应该按照肿瘤的生长动力学、大小和位置来对每位VHL、BDH和HPRCC患者进行主动监测(AS),而不是采用标准化的间隔随访。根据指南要求,定期对遗传性肾癌综合征患者的肾脏和肾外病变进行筛查。应酌情对遗传性肾癌综合征患者进行多学科讨论。 尽管体细胞TFE3和TFEB的融合易位是非遗传性的,但这可能影响15%的45岁以下肾癌患者和20-45%的确诊为肾癌的儿童和年轻人。 最近一项II期临床试验证明了口服MK-6482(HIF-2α抑制剂)在VHL患者中的临床效用。在被评估的61位VHL相关的肾癌患者中,应用MK-6482的客观缓解率(ORR)为28%,疾病稳定率(SDR)为71%,肿瘤直径中位数每年线性下降-6.4 mm(23.3-4.5)。一项独立评估发现,87%的患者的靶病灶较基线水平有所降低。这项研究仅进行了36周的随访,但取得的结果是令人满意的。目前这项研究结果还未得到验证。 对于年轻病人,在以下情况时建议进行遗传咨询:双侧多发肿瘤,既往有肾癌家族史以及罕见的肿瘤形态。 3.4.5 血管平滑肌脂肪瘤(Angiomyolipoma, AML) 血管平滑肌脂肪瘤(AMLs)是一种良性的间质肿瘤。它可以散发或作为结节性硬化症的一部分。AMLs的患病率为0.44%(女性为0.6%,男性为0.3%)。只有5%的患者中出现多发性AMLs。AMLs属于PEComas (血管周围上皮样细胞肿瘤perivascular epithelioid cell tumours,)。这种肿瘤的特征是血管周围上皮样细胞增生。部分PEComas肿瘤具有侵袭性,甚至可以远处转移。典型的AMLs是良性肿瘤。由于AMLs中存在有脂肪组织,超声、CT和MRI可以用于AMLs的诊断。但是对于脂肪含量较低的AMLs,诊断性成像并不能可靠地识别病变组织。经皮活检基本没有诊断价值。对于在初次诊断中不能确定良恶性的肾脏肿瘤,应按照本指南中关于肾癌治疗的推荐方案进行治疗。在结节性硬化症的病人中,如果在肿大淋巴结中发现AMLs,并不代表肿瘤的转移,而是提示多发性AMLs。在极少数病例中,可以发现非恶性瘤栓延伸至肾静脉或下腔静脉,这与血管营养型AMLs的生长相关。上皮样AMLs是一种非常罕见的变异型AML,其肿瘤组织至少80%由上皮样细胞组成。上皮样AMLs具有潜在恶性,但具有侵袭性肿瘤的患者比例变化很大。WHO 2016提出了预测上皮样AMLs生物学特性的标准。一般来说,AMLs生长缓慢而稳定,并且发病率最低。 在某些情况下,较大的AMLs会引起局部疼痛。AMLs的主要并发症是腹膜后或肾脏集合系统的自发性出血,可危及生命。出血是由肿瘤自发破裂引起的。关于出血的危险因素知之甚少。但人们认为出血风险会随着肿瘤大小的增加而增加。此外,出血风险的增加也可能可能与肿瘤血管有关,包括不规则血管的生成。出血的主要危险因素包括肿瘤的大小、肿瘤血管分级和结节性硬化。 3.4.5.1 治疗 大多数AMLs(48%)最适合的选择是主动监测(AS)。在一组主动检测的AMLs患者中, 11%的患者的肿瘤增长,2%的患者有自发出血,5%的患者采取积极治疗(LE: 3)。AMLs的大小和出血的风险之间的关系尚不清楚。以往以肿瘤直径达到4厘米为肿瘤切除的标准(4-cm cut-off)。但这(4-cm cut-off)本身不应该作为采取积极治疗的标准。当达到手术指征时,如果条件允许,应首选保留肾单位手术(NSS)。微创选择性动脉栓塞(SAE)的主要缺点是复发率更高以及需要二次治疗(手术0.85% vs SAE 31%)。有关热消融治疗AMLs的的研究数据不足,且这种方法的使用频率较低。 对于有持续性疼痛、肿瘤破裂(急性或反复出血)或瘤体较大的AMLs患者,应积极采取治疗(选择性动脉栓塞、手术或消融)。病人的具体情况可能会影响治疗方式的选择,例如腹部外伤风险高的患者、育龄期女性以及随访或急诊不到位的患者。AMLs患者出血危及生命时,可以进行选择性动脉栓塞。 在诊断为结节性硬化症的患者中,使用依维莫司抑制mTOR通路可缩小双侧AMLs的体积。这一结论已经在RCT研究中得到验证。在一项小规模的II期临床试验(n = 20)中,依维莫司对散发性AML的疗效也得到了证实。有55.6%(4个月)和71.4%(6个月)的患者的肿瘤体积缩小了25%及以上,20%的患者因药物毒性而退出研究,40%的患者因副作用而自行退出研究。 3.4.6 肾嗜酸细胞瘤(Renal oncocytoma) 肾嗜酸细胞瘤是一种良性肿瘤,占所有实体肾脏肿瘤的3%-7%。但在
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科3840人已读 - 医学科普 前列腺癌的骨转移5(治疗)
双膦酸盐是恶性肿瘤骨转移的基础用药。对于前列腺癌骨转移伴有骨痛的患者,双膦酸盐可减少和推迟mCRPC骨转移患者的骨相关事件发生。无论激素敏感型或去势抵抗型均应考虑使用双膦酸盐类药物进行治疗。 常用双膦酸盐药物用药方法:一般用12个月左右。(1)一代药物氯膦酸盐片1 600 mg/d口服,或静脉注射氯膦酸盐针300 mg/d,> 2 h/d持续5 d;(2)二代药物帕米膦酸盐90 mg,静脉注射 > 2 h,每3~4周一次;(3)三代药物唑来膦酸盐4 mg,静脉注射 > 15 min,每3~4周一次;禁用于肌酐清除率 < 35 ml/min的患者;因卡膦酸二钠10 mg,静脉注射2~4 h,每3~4周一次,65周岁以上患者推荐剂量为一次5 mg,肌酐清除率 < 30 ml/min的患者慎用或减量使用,并监测肾功能;伊班膦酸盐4 mg,静脉注射 > 2 h,肌酐清除率 < 30 ml/min的患者不建议使用,每3~4周一次。 常见不良反应及注意事项:双膦酸盐安全性良好,最常见的不良反应是流感样症状(如发热、疲乏、寒战及关节或肌肉疼痛等),临床上可采用乙酰氨基酚类退热处理及补液支持治疗。口服双膦酸盐类的不良反应还有食管炎、恶心、呕吐、腹泻等;一般对症处理即可。静脉注射的双膦酸盐类药物可导致肾脏毒性、低钙血症、颌骨坏死。其所致的急性肾衰竭通过透析等治疗往往是可以逆转的,然而临床上也有转为慢性肾病者,因此使用双膦酸盐时需注意避免与有肾功能损害作用的药物同时使用,同时注意监测肾功能、肌酐清除率。补充维生素D及钙剂可减少低钙血症的发生。定期监测电解质水平,对于肾功能不全的患者在使用双膦酸盐时应高度警惕低钙血症的发生。下颌骨坏死以预防为主,双膦酸盐的累积使用剂量及用药持续时间、拔牙或植牙手术史、牙周病史及感染病史均为其发生的高危因素,临床上应规范其使用时间和累积剂量。同时在初始治疗前应该进行口腔检查及预防性治疗,治疗期间也需要注意保持良好的口腔卫生。
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科1649人已读 - 医学科普 前列腺癌的骨转移2
前列腺癌骨转移以成骨性病灶为主。而且成骨性病灶以结构紊乱、不稳定的成骨性改变为主,并且成骨性改变和溶骨性改变同时存在。目前认为前列腺癌骨转移的发病机制主要有两种:一种是通过Baston脊椎静脉丛转移至脊柱。该学说主要认为脊椎静脉丛无静脉瓣,而且脊椎静脉丛与胸腔静脉丛、腹腔静脉丛、肋间静脉丛等彼此相通,此静脉压力低,当胸腹盆腔因各种原因导致压力增高时,静脉内的肿瘤细胞可以不经过肝、肺而直接进入Baston脊椎静脉丛,从而转移至脊椎和骨盆;另一种是基于Paget的种子和土壤学说。该学说认为,种子是前列腺癌细胞,土壤是骨骼。前列腺癌细胞与骨骼处于一种微环境中,骨微环境的固有生物学特性为前列腺癌细胞提供了着床的条件,同时前列腺癌细胞破坏骨基质降解释放的细胞因子反过来调控骨的微环境,刺激了前列腺癌细胞生长。近年研究还显示原发灶对转移灶的形成和发展起到促进作用,原发病灶分泌的细胞因子可能直接影响远处转移灶中的转移克隆生长,但具体作用机制仍在探索研究中。前列腺癌骨转移是多步骤、多环节的复杂生物学过程、多种趋化因子、整合素、黏附因子、细胞外基质、造血干细胞、间充质干细胞等均可能参与其中。
王哲 副主任医师 河北北方学院附属第一医院 泌尿外科952人已读





